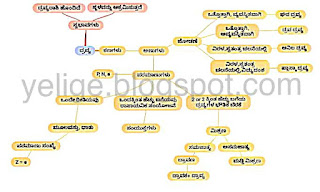
ದ್ರವ್ಯರಾಶಿಯನ್ನು ಹೊಂದಿರುವ ಹಾಗೂ ಸ್ಥಳವನ್ನು ಆಕ್ರಮಿಸುವ ಯಾವುದೇ ವಸ್ತುವನ್ನು ದ್ರವ್ಯ ಎನ್ನುತ್ತೇವೆ.
ದ್ರವ್ಯವು ಅಣುಗಳಿಂದ ಮಾಡಲ್ಪಟ್ಟಿದೆ.ದ್ರವ್ಯದ ಎಲ್ಲಾ ಮೂಲ ಗುಣಗಳನ್ನು ಹೊಂದಿದ ಸ್ವತಂತ್ರ ಕಣವನ್ನು ಅಣು ಎನ್ನುತ್ತೇವೆ.
ಅನುವು ಪರಮಾಣುಗಳ ಗುಚ್ಛವಾಗಿದೆ.ಒಂದು ಅಣುವಿ ನಲ್ಲಿರುವ ಎಲ್ಲಾ ಪರಮಾಣುಗಳ ರಾಶಿಗಳ ಮೊತ್ತಕ್ಕೆ ಅಣುರಾಶಿ ಎನ್ನುತ್ತೇವೆ.
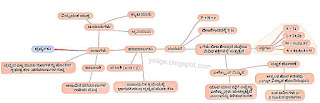
ರಾಸಾಯನಿಕ ಕ್ರಿಯೆಯಲ್ಲಿ ಭಾಗವಹಿಸಬಲ್ಲ ದ್ರವ್ಯದ ಮೂಲ ಕಣಕ್ಕೆ ಪರಮಾಣು ಎನ್ನುತ್ತೇವೆ.ಪರಮಾಣು ಪ್ರೋಟಾನ್ ನ್ಯೂಟ್ರಾನ್ ಎಲೆಕ್ಟ್ರಾನ್ ಗಳಿಂದ ಮಾಡಲ್ಪಟ್ಟಿದೆ.ಒಂದು ಪರಮಾಣುವಿನಲ್ಲಿರುವ ಪ್ರೋಟಾನ್ಗಳು ಮತ್ತು ನ್ಯೂಟ್ರಾನುಗಳ ರಾಶಿಗಳ ಮೊತ್ತಕ್ಕೆ ಪರಮಾಣು ರಾಶಿ (A) ಎನ್ನುತ್ತೇವೆ.ಪರಮಾಣು ರಾಶಿಯ ಏಕಮಾನ amu ಆಗಿದೆ (ಕಾರ್ಬನ್-12 ಪರಮಾಣುವಿನ ದ್ರವ್ಯರಾಶಿಯ 1/12).
ಪರಮಾಣುವಿನ ಬೀಜಕೇಂದ್ರ ದಲ್ಲಿ ಪ್ರೋಟಾನ್ಗಳು ಮತ್ತು ನ್ಯೂಟ್ರಾನ್ ಗಳು ಬಂಧಿಸಲ್ಪಟ್ಟಿರುತ್ತವೆ.
ಎಲೆಕ್ಟ್ರಾನ್ ಗಳು ಬೀಜ ಕೇಂದ್ರದ ಸುತ್ತಲೂ ವಿವಿಧ ಕಕ್ಷೆಗಳಲ್ಲಿ ಸುತ್ತುತ್ತಿರುತ್ತವೆ.ಕಕ್ಷೆಗಳನ್ನು K,L,M,N ಕಕ್ಷೆಗಳು ಎಂದು ವರ್ಗೀಕರಿಸಲಾಗಿದೆ. K ಕಕ್ಷೆಯು 1s ಎಂಬ ಉಪಕಕ್ಷೆ ಹೊಂದಿದೆ. L ಕಕ್ಷೆಯು 2s,2p ಎಂಬ ಉಪ ಕಕ್ಷೆಗಳನ್ನು ಹೊಂದಿದೆ.M ಕಕ್ಷೆಯು 3s,3p,3d ಎಂಬ ಉಪ ಕಕ್ಷೆಗಳನ್ನು ಹೊಂದಿದೆ.
N ಕಕ್ಷೆಯು 4s,4p,4d,4f ಎಂಬ ಉಪ ಕಕ್ಷೆಗಳನ್ನು ಹೊಂದಿದೆ.
ಎಲೆಕ್ಟ್ರಾನ್ ವಿನ್ಯಾಸ ;
ಯಾವ ಯಾವ ಕಕ್ಷೆಗೆ ಎಷ್ಟೆಷ್ಟು ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಹಂಚಲ್ಪಟ್ಟಿವೆ ಎಂಬುದನ್ನು ತಿಳಿಸುವ ಬರಹಕ್ಕೆ ಎಲೆಕ್ಟ್ರಾನ್ ವಿನ್ಯಾಸ ಎನ್ನುತ್ತೇವೆ.
ಒಂದು ಪ್ರಧಾನ ಕಕ್ಷೆಯಲ್ಲಿ 2n² ರಷ್ಟು ಎಲೆಕ್ಟ್ರಾನ್ ಗಳು ತುಂಬಲ್ಪಡುತ್ತವೆ.ಇಲ್ಲಿ n ಎಂಬುದು ಪ್ರಧಾನ ಕಕ್ಷೆಯ ಸಂಖ್ಯೆಯಾಗಿದೆ.
ಅತ್ಯಂತ ಹೊರ ಕವಚವು ns²np⁶ ವಿನ್ಯಾಸ ಹೊಂದಿರುವುದನ್ನು ಅಷ್ಟಕ ಜೋಡಣೆ ಎನ್ನುತ್ತೇವೆ.ಅಷ್ಟಕ ಜೋಡಣೆಯನ್ನು ಹೊಂದಿರುವ ಧಾತುಗಳನ್ನು ಜಡ ಅನಿಲಗಳು ಅಥವಾ ಸೊನ್ನೆ ಗುಂಪಿನ ಧಾತುಗಳು ಎನ್ನುತ್ತೇವೆ.
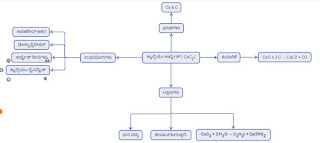
ಒಂದು ಅಣು ಅಥವಾ ಪರಮಾಣು ಎಲೆಕ್ಟ್ರಾನ್ ಅನ್ನು ಕಳೆದುಕೊಂಡಾಗ ಅಥವಾ ಪಡೆದುಕೊಂಡಾಗ ವಿದ್ಯುತ್ ಅಂಶಯುಕ್ತ ಕಣ ವಾಗುತ್ತದೆ.ಈ ಕಣಗಳನ್ನು ಅಯಾನುಗಳು ಎನ್ನುತ್ತೇವೆ.
ಅಣು ಅಥವಾ ಪರಮಾಣು ಎಲೆಕ್ಟ್ರಾನ್ ಅನ್ನು ಪಡೆದುಕೊಂಡು ಉಂಟಾದ ಅಯಾನು ಗಳಿಗೆ ಆ್ಯನಯಾನು ಎನ್ನುತ್ತೇವೆ.
ಅಣು ಅಥವಾ ಪರಮಾಣು ಎಲೆಕ್ಟ್ರಾನ್ ಅನ್ನು ಕಳೆದುಕೊಂಡು ಉಂಟಾದ ಅಯಾನು ಗಳಿಗೆ ಕ್ಯಾಟಯಾನು ಎನ್ನುತ್ತೇವೆ.